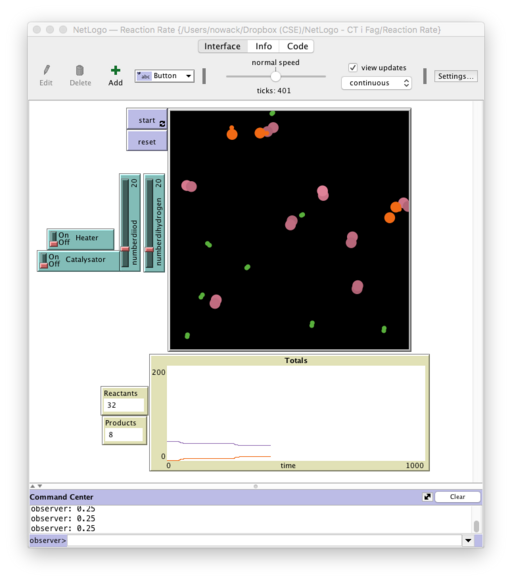
Der tages udgangspunkt i emnerne Reaktionshastighed i kemi. Disse emner kan forekomme abstrakte for eleverne, og håbet er at CT kan være med til at eleverne får en bedre forståelse af de central begreber i emnerne. Derfor bruges modeller i NetLogo (et agentbaseret programmeringsmiljø) til simulering af kemisk reaktionshastighed.
Ved at anvende agentbaseret modellering er det tydeligere for eleverne hvordan elementerne (agenterne) skabes og hvilke egenskaber og opførsel de har. Eleverne kan følge en agent (f.eks et dihydrogenmolekyle), både i interface'et og i code'en og der ved afgøre om agentens opførelse og egenskaber er i overensstemmelse med den faglige teori i faget.
Eleverne har herved mulighed for at se effekten af, hvad der sker på det mikroskopiske niveau, i det makroskopiske niveau, og for at se hvad et indgreb på det mikroskopiske niveau betyder for det makroskopiske fænomen.
Modellen og forløbet er udviklet for at fremme indlæring i emnet reaktionshastighed.
Det er håbet at eleverne bliver mere bevidste om, og arbejder med, deres egen mentale model af fænomenet undervejs, og at underviseren får et indblik i elevernes mentale modeller af fænomenet.
Der fokuseres på nogle af de faktorer der påvirker reaktionshastigheden af en kemisk reaktion. Det drejer sig om kvalitative beskrivelser frem for kvantitative (reaktionskinetik). Nedenfor er de faglige mål for eleverne beskrevet kort.
Reaktanternes koncentration: Et øget antal reaktanter giver en øget reaktionshastighed (flere sammenstød pr. tid vil give en øget reaktionshastighed)
Temperatur: En øget temperatur giver en øget reaktionshastighed (jo højere temperatur → jo højere gennemsnitlig kinetisk energi har partiklerne, dvs. jo højere hastighed → jo voldsommere sammenstød mellem partiklerne → jo flere sammenstød vil have energi nok til at klare ”energi-bjerget” (aktiveringsenergi) → jo flere reaktioner pr. tid)
Katalysator: Tilsætning af katalysator giver en øget reaktionshastighed (nedsætter størrelsen af ”energi-bjerget” (aktiveringsenergi) således at flere sammenstød ved den pågældende temperatur har energi nok til at reaktionen sker → jo flere reaktioner pr. tid).
Eleverne vil arbejde med modellen og tilhørende arbejdsspørgsmål i en dobbeltlektion som er to gange 45 minutter.
Emnet Reaktionshastighed er normalt en del af kemi på B-niveau.
Eleverne skal have adgang til egen eller skolens computer samt netadgang. Desuden skal eleverne arbejde med molekyl-byggesæt for at løse første arbejdsspørgsmål. Der kræves ingen erfaring med programmering for at deltage i forløbet.
Forløbet er struktureret i tre logiske klumper fordelt på introduktion, arbejdsopgaver og evalueringsspørgsmål og på perspektivering.
Introduktion til emnet:
Eleverne introduceres til reaktionshastighed (definition samt video Brainiac alkali metals https://www.youtube.com/watch?v=m55kgyApYrY)
Dernæst udfører eleverne forskellige små forsøg som illustrerer forskelle i reaktionshastighed (eksempelvis er redox-forsøg velegnede) (kommentar 9/8: evt demonstrationsforsøg pga. stort tidsforbrug ved elevforsøg)
Eleverne præsenteres for reaktionen mellem dihydrogen og diiod teoretisk.
Arbejdsopgaver til eleverne:
Eleverne arbejder i to-mands-grupper med modellen og individuelt med et spørgeskema der stilladserer deres arbejde med faget og modellen. Desuden indeholder spørgeskemaet nogle evaluerende spørgsmål som vurderer udbyttet af både det faglige og af computational thinking.
Opfølgning på elevernes arbejde på klassen
Indledende spørgsmål:
Byg følgende reaktion med molekylebyggesæt og beskriv hvad der sker i reaktionen: H2(g) + I2(g) <-> 2HI(g)
Hvad menes der med "reaktionshastighed"?
Hvilke faktorer kunne man forestille sig at reaktionshastighed afhænger af? Opstil nogle hypoteser ift. temperatur, katalysator og koncentrationen af reaktanter.
Hvad tror du, at man kan bruge computerbaserede modeller af kemiske reaktioner til?
Prøv modellen. Bare prøv dig frem. Der kan ikke gøres noget forkert. Hvis modellen pludselig opfører sig mærkeligt, kan du altid lukke den og downloade den igen.
Modellen og den kemiske reaktion:
Beskriv modellen og forklar hvad du tror de forskellige elementer repræsenterer.
Hvilke farver og størrelser har molekylerne?
Hvis du skulle ændre på nogle af molekylernes farver, hvilke farver ville du så vælge og hvorfor?
Hvis du skulle ændre på nogle af molekylernes størrelser, hvilke størrelser ville du så vælge til hvilke molekyler og hvorfor?
Interface og kode:
Prøv at finde ud af hvordan molekylerne får bestemte farver. Hvor og hvordan står det beskrevet i code-fanen?
Prøv at finde ud af hvordan molekylerne får bestemte størrelser. Hvor og hvordan står det beskrevet i code-fanen?
Prøv at ændre molekylernes farve og størrelse, som du foreslog i det tidligere spørgsmål. Hvor godt lykkedes det for dig og hvordan gjorde du?
Modellen:
Vær sikker på at du har kørt modellen tilstrækkeligt mange gange, inden du besvarer nedenstående spørgsmål. Hvilken betydning har temperaturen for reaktionshastigheden? Hvilken betydning har tilsætning af en katalysator for reaktionshastigheden, og hvilken betydning har koncentrationen af reaktanter for reaktionshastigheden?
Beskriv hvordan modellen passer med dine hypoteser for reaktionshastighed ift. temperatur, katalysator og reaktanters koncentration.
Hvad menes der med "Reaktionshastighed" og hvilke faktorer afhænger reaktionshastigheden af?
Er arbejdet med modellen en god måde at introducere emnet Reaktionshastighed?
Eleverne skal starte med at downloade Netlogo og derefter se nedenstående to videoer. Netlogo kan hentes her: http://ccl.northwestern.edu/netlogo/
Introduktion til Netlogo
Introduktion til model interfacet
Netlogo modellen kan hentes her:
Introduktionsvideo
Løsningsvideo
F.eks.
Basiskemi B, 2014, Helge Mygind, Vibeke Axelsen, Ole Vesterlund Nielsen, Haase Forlag
Perspektivering:
Nedenstående links er ikke en del af NetLogo modellen, men kan bruges i forløbet efterfølgende.
Eleverne kan lege med modellerne og beskrive hvor modellerne er gode eller dårlige, samt hvordan de er kommet frem til denne vurdering. Derefter kan man få en snak om, hvordan modellerne skulle ændres for at blive bedre - og om de kan ændres (i modsætning til NetLogo modellerne).
Kollision og reaktion samt temperatur og reaktionshastighed: (http://www.physics-chemistry-interactive-flash-animation.com/chemistry_interactive/chemical_kinetics_factor_temperature.htm)
Diverse PHET-simuleringer (Colorado University). Reaktionshastighed (Reactions & Rates) og ligevægt (Reversible Reactions) https://phet.colorado.edu/en/simulations/category/chemistry/general